【中信新三板医药】新三板医药行业日报(20170323)―FDA批准帕金森病新药,放射性药品经营审批等被取消(2)
2017-03-24 编辑:
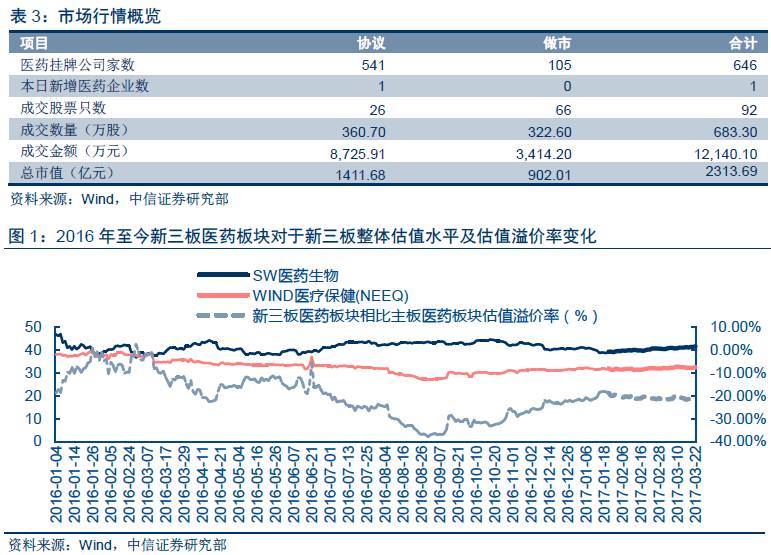
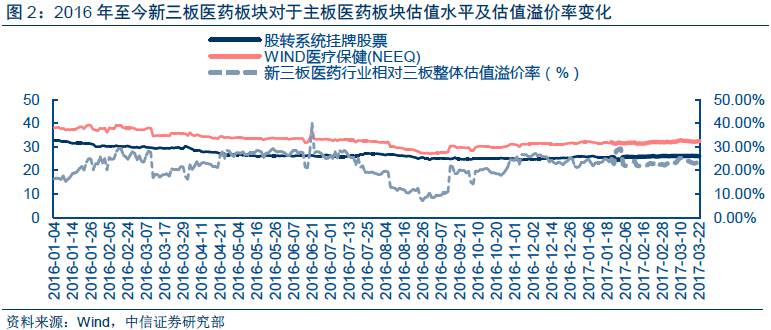
市盈率方面(TTM,整体法剔除负值),截止2017年3月22日,新三板医药板块估值水平为32X,与上一交易日持平。新三板整体估值水平为26X,与上一交易日持平。溢价率方面,新三板医药板块对于新三板挂牌企业整体的估值溢价率为24%;新三板医药板块对于主板医药板块折价22%。
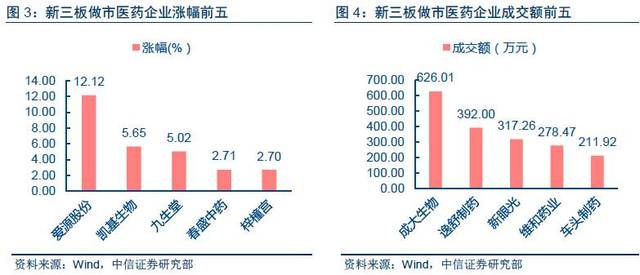
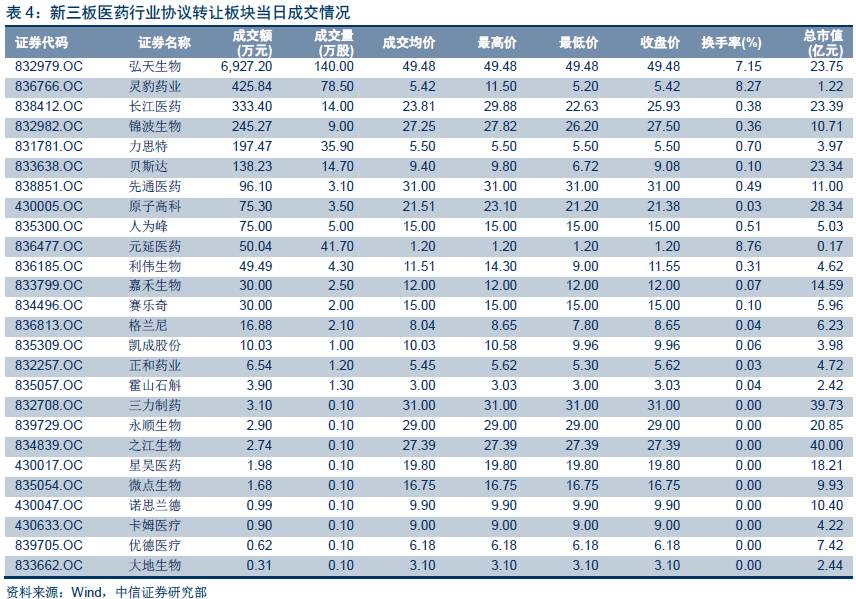
(1)做市转让板块,2017年3月22日共有28只股票上涨,涨幅最高的爱源股份、凯基生物、九生堂分别上涨12.12%/5.65%/5.02%。做市板块成交额最高的前三位分别是成大生物、逸舒制药、新眼光,成交额分别为626.01/392/317.26万元。
(2)协议转让板块,2017年3月22日医药企业成交26家,成交额最高的前三位分别为弘天生物、灵豹药业、长江医药,成交额分别为6927.2/425.84/333.40万元。
新增挂牌公司及中信证券研究部新三板医药覆盖股票
2017年3月22日新增挂牌医药企业1家。绿金高新属于生物肥及有机化学农药生产企业。根据2015年年报数据,公司营业收入2146.15万元,同比下降20.98%;盈利方面,2015年公司亏损347.81万元。
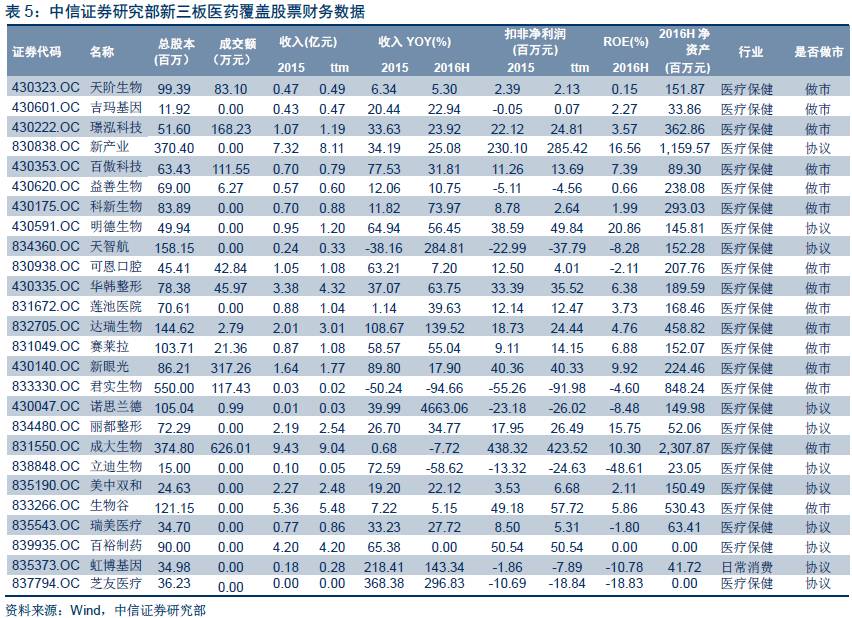
中信证券研究部新三板团队总共重点覆盖医药公司26家。成交方面,成大生物单日成交额最大,为626.01万元。
新三板医药行业每日定增融资回顾
3月22日新三板医药行业兰卫检验实施定向增发,实际募资总额5.33亿元,募资后PE(TTM)为34X。2016年至今新三板医药板块实际募资总额达120亿元。
医药行业每日新闻
国内新闻:国务院修改和废止部分行政法规,放射性药品经营审批等34项被取消
重点综合医讯:
1.国务院修改和废止部分行政法规,放射性药品经营审批等34项被取消。国务院总理李克强签署第676号国务院令,公布《国务院关于修改和废止部分行政法规的决定》,自公布之日起施行。在医疗方面,通过修改放射性药品管理办法等22部行政法规的68个条款,取消了放射性药品经营审批等34项审批项目。(信息来源:健康报)
2.2017年2月份总局批准39个医疗器械上市。2017年2月,国家食品药品监督管理总局共批准注册医疗器械产品39个。其中,境内第三类医疗器械产品28个,进口第三类医疗器械产品2个,进口第二类医疗器械产品9个。(信息来源:CFDA)
3.宁夏银川互联网医院就医问诊产生的费用可由本人医保账户资金支付并按比例报销。银川出台新规,为推进“互联网+医疗”产业发展,建立健全多层次医疗保障体系,明确建立参保人员网上门诊统筹医疗保险试点制度,参保人员在互联网医院就医问诊产生的费用,可由本人医保账户资金支付并按比例报销。(信息来源:新华社)
4.贵州:贫困人口13种大病免费治。《贵州省农村贫困人口大病专项救治工作实施方案》日前印发,通过基本医保、大病保险和医疗救助制度的紧密衔接,对符合该省7类13种大病临床路径的专项救治对象实行免费救治。此次列入的疾病包括:儿童白血病(含急性淋巴细胞白血病和急性早幼粒细胞白血病)、儿童先天性心脏病(含房间隔缺损、室间隔缺损、动脉导管未闭、肺动脉瓣狭窄、法式四联征以及合并两种或以上的复杂性先心病)、食管癌、胃癌、结肠癌、直肠癌、终末期肾病。(信息来源:新华网)
海外新闻:FDA批准帕金森病新药,礼来乳腺癌在研新药取得3期研究成功
重点综合医讯:
1.美国FDA今日批准十年来首个帕金森病新药。由意大利赞邦集团(Zambon)及Newron制药公司合作研发的帕金森药物Xadago(safinamide)获美国FDA批准上市,这也是美国在十多年来首个获批用于治疗帕金森病的新化学实体(New Chemical Entity)。(信息来源:医谷)
2.礼来乳腺癌在研新药取得3期研究成功。礼来公司新药MONARCH 2临床试验中乳腺癌在研新药abemaciclib达到了无进展生存期(PFS)的主要终点。这项3期研究评价了细胞周期蛋白依赖性激酶(CDK)4和CDK6抑制剂abemaciclib与fulvestrant联合治疗激素受体阳性(HR +)、人表皮生长因子受体2阴性(HER2-)晚期乳腺癌的功效和安全性,这些妇女患者在内分泌治疗后病情复发或进展。结果表明,当与安慰剂加上fulvestrant的对照组相比较时,abemaciclib和fulvestrant的联合治疗方案取得了统计学上PFS的显著改善。(信息来源:药明康德)
3.韩生物技术公司研制出一种治疗阿尔茨海默症的自体脂肪干细胞疗法。韩国生物技术公司Nature Cell宣布,该公司旗下干细胞研究机构Biostar在美国已经开始开展一项名为“ASTROSTEM”的干细胞药物的I/II期临床试验,现在正在招募阿尔茨海默症(AD)的患者。该公司CEOJeongchan Ra博士表示,这项研究的I/II期临床试验已于2016年11月24日获得美国FDA的批准。这款名为“AstroStem”干细胞药物是从收集的10克成人腹部皮下脂肪组织中分离得到的一种具有多向分化潜能的干细胞,然后再通过静脉注射10次,每次2亿个细胞,输入到病人体内。(信息来源:医谷)